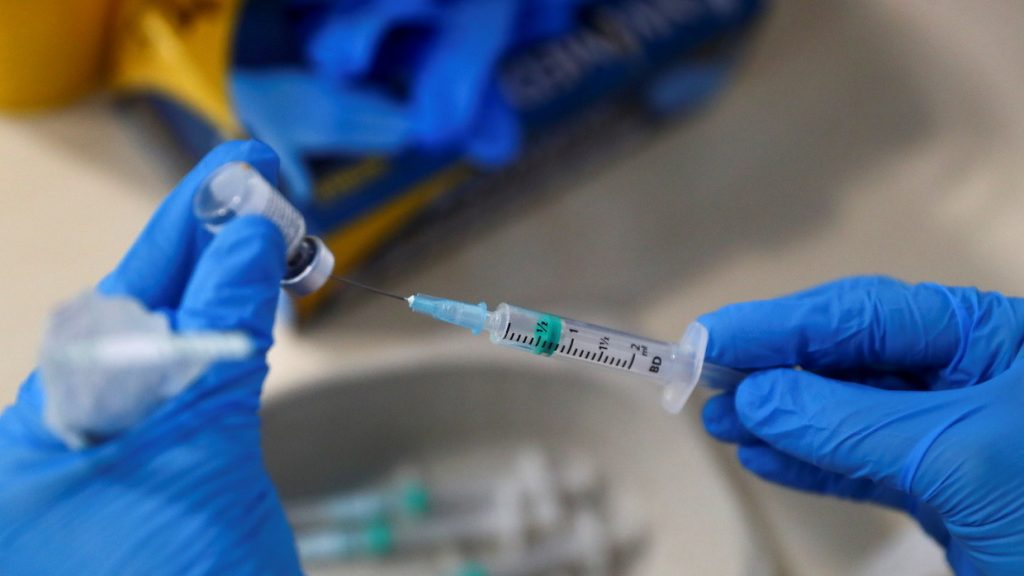
Une infirmière remplit une seringue avec une dose de vaccin Pfizer
Pfizer dit avoir retiré sa demande d’autorisation d’utiliser son vaccin Covid-19 en Inde. L’entreprise a promis de soumettre à nouveau la demande dès qu’elle aura rassemblé davantage de données.
Le fabricant de médicaments basé aux États-Unis a déclaré que la décision a été prise après une réunion avec un groupe d’experts de l’autorité de régulation de l’État indien mercredi.
« Sur la base des délibérations de la réunion et de notre compréhension des informations supplémentaires dont l’organisme de réglementation pourrait avoir besoin, la société a décidé de retirer sa demande pour le moment », a déclaré le porte-parole de Pfizer dans un communiqué.
L’entreprise a ajouté qu’elle « soumettra à nouveau sa demande d’approbation avec des informations supplémentaires dès qu’elles seront disponibles dans un avenir proche ».
Le journal Economic Times a cité une source gouvernementale disant que Pfizer voulait une dérogation pour les essais cliniques de son vaccin, développé conjointement avec la firme allemande BioNTech, mais le régulateur a insisté pour qu’une étude complémentaire soit réalisée en Inde. Les experts voulaient voir comment le vaccin fonctionnerait au sein de la population indienne avant qu’il ne soit autorisé pour une utilisation générale dans le pays, a expliqué la source.
Vinod K. Paul, le chef d’un panel gouvernemental sur la stratégie des vaccins, a déclaré à Reuters plus tôt ce mois-ci qu’un essai de transition en Inde est une « condition préalable » pour que tout vaccin soit autorisé dans le pays.
L’Inde a lancé une campagne de vaccination nationale le 16 janvier, en utilisant une version fabriquée localement du vaccin AstraZeneca-Oxford et un vaccin appelé Covaxin, fabriqué par une société pharmaceutique indienne, Bharat Biotech.




